RPS Cas du Mois
Déc 2023
Découverte inattendue chez un homme de 65 ans atteint d'une maladie rénale chronique et d'une protéinurie minime
Siarhei Dzedzik1
Ilya Glezerman1,2
Surya V. Seshan1
1. New York-Presbyterian/Weill Cornell Medicine, New York, NY2. Memorial Sloan Kettering Cancer Center, New York, NY
HISTOIRE CLINIQUE
Homme de 65 ans qui s'est initialement présenté à l'hôpital local après une chute. L’étude d’imagerie a révélé une lésion ostéolytique avec suspicion de fracture pathologique du corps vertébral C6. Après résection de la lésion, le patient a reçu une radiothérapie dans la zone touchée. L'examen pathologique a montré des cellules tumorales positives pour CD138 avec restriction kappa, ce qui concorde avec le diagnostic de plasmocytome. Deux ans et demi plus tard, il est évalué pour une créatinine élevée, qui est passée d'une valeur de base de 1,0 (N = 0,6-1,3) mg/dl à 1,5 mg/dL. L'examen physique est sans particularité. Un panel métabolique complet est également sans particularité. De plus, il y avait une élévation des chaînes légères kappa libres à 38,09 (0,33-1,94) mg/dL, un rapport kappa/lambda de 35,93 (0,26-1,65), l'électrophorèse des protéines sériques est négative pour un pic monoclonal et l'immunofixation sanguine positive pour une gammapathie monoclonale à IgA kappa. L'électrophorèse des protéines urinaires est négative pour un pic monoclonal, mais l'immunofixation urinaire est positive pour la bande de chaîne légère kappa libre monoclonale. Le rapport protéine/créatinine urinaire (UPC) est inférieur à 0,1 et l'analyse d'urine était dépourvue de cellules et de sédiments. Initialement, le patient est suivi de manière conservative mais une biopsie rénale dix mois après la présentation clinique initiale est réalisée en raison de l'augmentation des chaînes légères kappa libres (84,07 mg/dL) et du développement d'une protéinurie avec un ratio protéines/créatinine urinaires de 0,6.
RÉSULTATS DE LA BIOPSIE RÉNALE
La microscopie optique révèle de légères modifications ischémiques dans neuf glomérules sur quarante-sept (9/47). Les glomérules restants sont sans particularité. Près de 30 % du tissu cortical présente une atrophie tubulaire avec une légère fibrose interstitielle et des infiltrats inflammatoires interstitiels chroniques minimes à clairsemés, composés de lymphocytes mélangés à des macrophages dispersés et occasionnellement des plasmocytes. La morphologie tubulaire est résumée dans la figure 1. 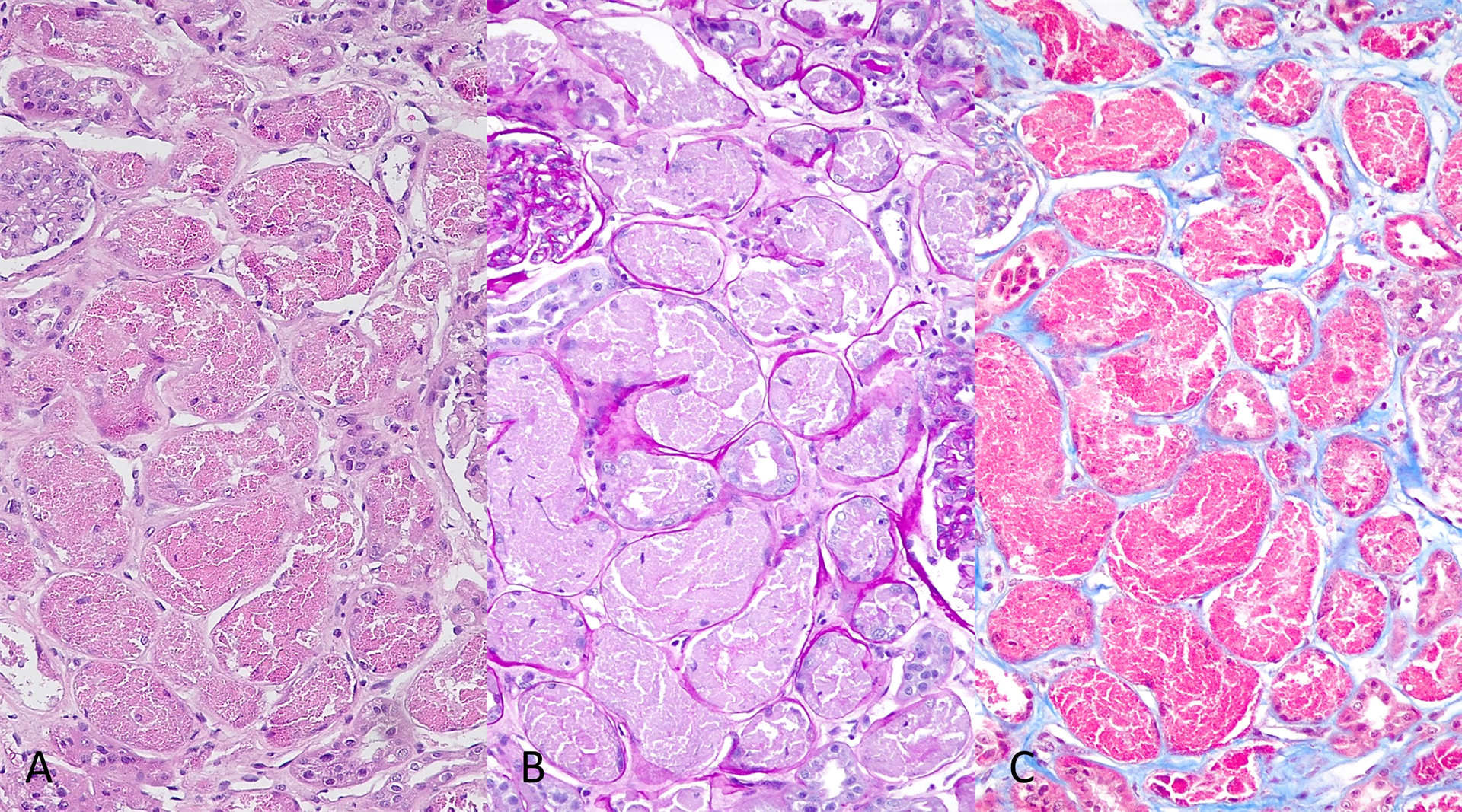
Figure 1: La plupart des tubules proximaux semblent hypertrophiés. Les cellules épithéliales sont distendues par un matériel éosinophile grossièrement granuleux (A) qui est négatif au PAS (B) et fortement fuchsinophile sur la coloration trichrome (C). Il existe des lésions épithéliales tubulaires qui vont de la perte de la bordure en brosse, à la caryopycnose, à la perte de cohésion cellulaire et à leur desquamation subséquente dans la lumière.
MICROSCOPIE PAR IMMUNOFLUORESCENCE (IF) :
La microscopie par immunofluorescence (2 glomérules), réalisée sur tissu congelé (IF-C), n'a révélé aucune coloration des immunoglobulines IgG, IgA, des composants du complément C3, C1q, des chaînes légères kappa et lambda au sein des glomérules, du compartiment tubulo-interstitiel et des vaisseaux artériels. L’immunofluorescence, réalisée sur des tissus inclus en paraffine fixés au formol digérés par la protéase (IF-P), est illustrée à la figure 2.
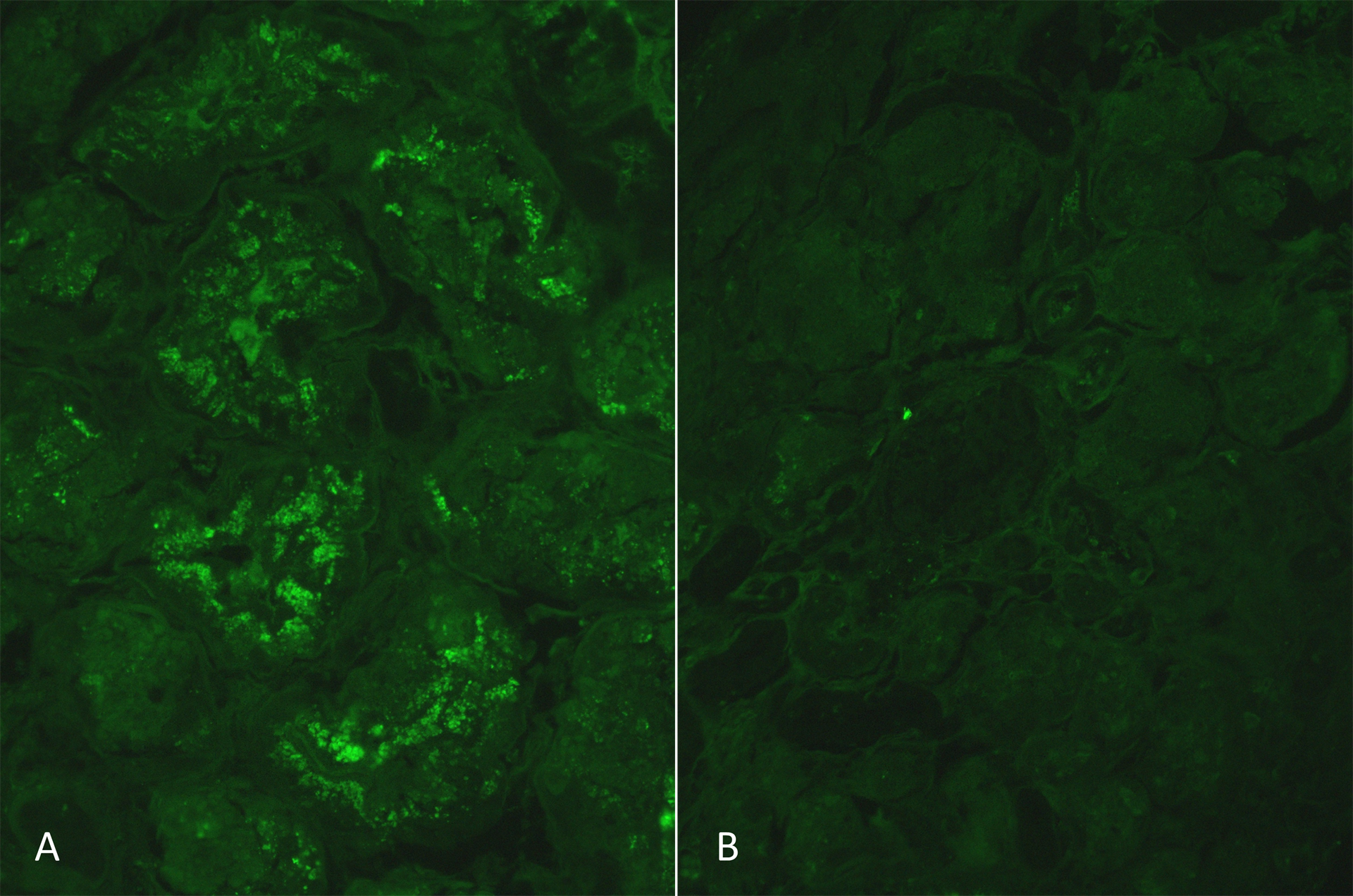
Figure 2: L’IF-P utilisant des anticorps anti-chaînes légères humaines kappa et lambda conjugués au FITC montre une coloration positive de 1 à 2+ pour les chaînes légères kappa principalement dans les cellules tubulaires (A). Une positivité occasionnelle des cellules épithéliales glomérulaires a également est notée (non présentée ici). Aucune coloration des chaînes légères lambda n'est notée dans les cellules tubulaires (B).
MICROSCOPIE ÉLECTRONIQUE (ME):
En ME, les podocytes présentent de rares vacuoles arrondies, dispersées et denses en électrons. Les processus du pied sont généralement préservés. Les cellules endothéliales présentent un léger gonflement avec perte de fenestration. Les membranes basales capillaires sont normales, avec une épaisseur allant de 300 à 350 nm. Les zones mésangiales présentent une légère augmentation segmentale de la matrice avec une cellularité normale. Aucun dépôt de complexe immun n'est identifié dans les membranes basales capillaires glomérulaires ou dans les zones mésangiales. Les résultats tubulaires pertinents sont résumés dans la figure 3.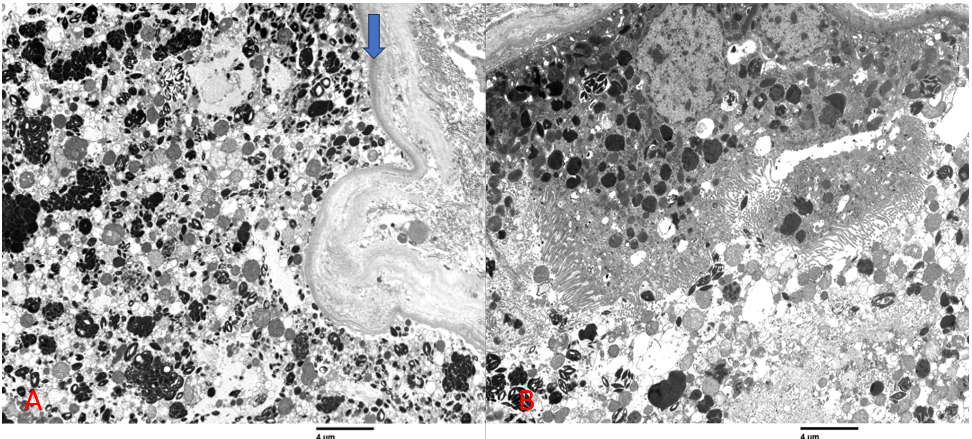
Figure 3. Les cellules épithéliales tubulaires proximales sont variablement gonflées et contiennent des lysosomes proéminents avec des inclusions dense aux électrons (A; la flèche bleue marque la membrane basale tubulaire), dont certaines ont des configurations cristallines (B) ou comme des corps myéliniques. Plusieurs cristaux sont visibles dans la lumière tubulaire (B).
DIAGNOSTIC FINAL
- Tubulopathie proximale des chaînes légères, principalement non cristalline, mais aussi focalement de type cristallin, associée aux chaînes légères monoclonales kappa, et avec atteinte épithéliale glomérulaire occasionnelle.
- Atrophie tubulaire focale avec légère fibrose interstitielle, 30% du cortex.
- Légers changements ischémiques globaux et glomérulosclérose globale.
- Aucune preuve concomitante de maladie de dépôt d'immunoglobulines monoclonales, de néphropathie à cylindres myélomateux ou d'amylose.
DISCUSSION
La gammapathie monoclonale est définie par la détection d’une chaîne lourde monoclonale, de chaînes lourdes et légères, ou d’une chaîne légère kappa ou lambda isolée dans la circulation. Celle-ci est la conséquence d’une production anormale d’immunoglobulines monoclonales ou de leurs composants. La source de protéines monoclonales (paraprotéines) va des lymphomes indolents à cellules B aux néoplasmes plasmocytaires. Le spectre de la présentation clinique varie également – depuis des entités de bas grade ne nécessitant pas de traitement (MGUS) jusqu’à des maladies évolutives de mauvais pronostic. Ces paraprotéines peuvent se déposer dans divers organes, provoquant des lésions tissulaires. En ce qui concerne le rein, le terme gammapathie monoclonale de signification rénale (MGRS) a été introduit pour souligner la mise en évidence de lésions rénales liées à la paraprotéinémie monoclonale malgré l'absence de critères diagnostiques d'une tumeur hématologique [1]. Il a été démontré que la maladie rénale chez les patients atteints de gammapathie monoclonale ou de myélome multiple est associée à un plus mauvais pronostic [2], qui peut être amélioré par une chimiothérapie visant la réduction rapide des chaînes légères (LC) en contrôlant le clone néoplasique [3].
Les lésions rénales sous MGRS comprennent généralement l'amylose AL ou la maladie des dépôts d'immunoglobulines monoclonales, qui impliquent également le tubulo-interstitium et le système vasculaire. La tubulopathie proximale des chaînes légères (TPCL) est un représentant rare de ce groupe, représentant 4 à 5 % des MGRS (Tableau 1) [4, 5]. Une présentation clinique typique de la TPCL est une protéinurie non néphrotique avec une protéine médiane de 1,5 à 2,5 g/jour ou une maladie rénale chronique légère (créatinine médiane de 1,9 à 2,0 mg/dl) [6]. Un syndrome de Fanconi complet ou incomplet est détecté dans environ 40 % des cas [4]. La protéinurie de Bence Jones est presque toujours présente.
Plusieurs formes morphologiques de TPCL sont décrites, cependant, elle est communément divisée en type cristallin et non cristallin [5, 7]. Le type cristallin est caractérisé par des inclusions cristallines intracellulaires de différentes tailles et formes - rectangulaires, rhomboïdes, en forme d'aiguille, etc. Elles ont tendance à s'accumuler dans les lysosomes de l'épithélium tubulaire proximal, provoquant des lésions cellulaires et interférant avec leur fonction. Les chaînes légères monoclonales sont librement filtrées dans le glomérule et réabsorbées par les cellules épithéliales tubulaires proximales via le récepteur ou complexe mégaline/cubiline, suivies de leur dégradation intralysosomale. Dans la TPCL, cependant, les chaînes légères anormales possèdent des chaînes latérales d'acides aminés hydrophobes en raison de mutations dans le domaine variable de la molécule d'immunoglobuline, qui leur confèrent la capacité de résister à la dégradation des enzymes lysosomales et de la protéase. De tels cristaux ou inclusions de chaînes légères perturbent la fonction lysosomale, induisant des lésions cellulaires, altérant la réabsorption, ce qui entraîne une tubulopathie proximale des chaînes légères [8]. Plus de 90 % des LC provoquant la TPCL appartiennent au sous-groupe 1 du domaine variable kappa. En revanche, la plupart des cas de TPCL lambda sont de type non cristallin car les LC lambda n'ont pas la capacité de cristalliser spontanément [9]. Les podocytes peuvent parfois présenter une accumulation d'inclusions cristallines en cas de TPCL de type cristallin, conduisant à une protéinurie de rang néphrotique [4]. Des structures podocytaires non cristallines ont été identifiées dans notre cas. L’importance de ces vacuoles denses en électrons est inconnue. Elles peuvent soit représenter une observation non spécifique reflétant une protéinurie de faible niveau, soit être liées à la protéine monoclonale. La TPCL est un défi diagnostique étant donné sa rareté et seulement une fraction des patients a une maladie hématologique déjà connue lors de la présentation initiale, allant de 15 % à 50 % au moment de la biopsie rénale [4, 5, 10]. Un autre défi est le résultat fréquemment faussement négatif des études en immunofluorescence des chaînes légères, lorsque celles-ci sont réalisées sur des tissus congelés. Une étape de démasquage antigénique utilisant la digestion enzymatique peut être nécessaire pour exposer les épitopes spécifiques afin d'obtenir une coloration positive [11]. La sensibilité de l'IF-C et de l'IF-P pour la détection de la TPCL est respectivement de 35 % (15/43) et 97 % (37/38). Il est intéressant de noter que l’IF-C est meilleure pour détecter la TPCL non cristalline que la TPCL cristalline de manière significative [4].
Bien que des dépôts de chaînes légères monoclonales cristallines et non cristallines puissent coexister, les dépôts cristallins ne peuvent souvent être reconnus que par un examen ultrastructurel, la microscopie optique montrant principalement un matériel grossièrement granuleux dans les tubules proximaux et ne montrant pas de structures cristallines claires [4]. Ceci est démontré dans le cas présenté ici (voir ci-dessus les résultats de la microscopie optique et électronique). Cependant, un doute est soulevé quant à savoir si le type non cristallin de TPCL représente un processus pathologique véritablement indépendant ou s'il s'agit simplement d'un trafic physiologique de chaînes légères [5, 12]. La formation focale de cristaux dans notre cas ne reflète pas l'étendue ou la gravité des dommages tubulaires observés en microscopie optique et corroborés par les données de laboratoire. Ceci suggère que le composant non cristallin de la TPCL est responsable d'une grande partie du dysfonctionnement épithélial tubulaire proximal conduisant à une insuffisance rénale aiguë (IRA).
Le pilier du traitement de la MGRS consiste à contrôler le clone néoplasique par chimiothérapie ou par transplantation de cellules souches - des approches qui n'étaient auparavant utilisées que chez les patients ayant un diagnostic établi de malignité hématologique. La réduction des chaînes légères libres chez les patients atteints de gammapathies monoclonales est associée à une amélioration de la fonction rénale plus probante, entraînant une amélioration de la survie des patients [13].|
Épidémiologie et manifestations rénales |
Microscopie optique |
Immunofluorescence |
Microscopie électronique |
|
|
Light chain cast nephropathy |
Néphropathie à cylindres à chaînes légères chez 33 % des patients atteints de myélome multiple [14]. IRA (DFGe médian : 13 mL/min/1,73 m2), protéinurie non albuminique (protéine urinaire médiane sur 24 h : 2,2 g et excrétion urinaire médiane d'albumine : 9 %), IRC progressive. |
Cylindres franchement éosinophile, rose pâle au PAS, fuscinophile en coloration trichrome dans les segments distaux du néphron. Les cylindres sont anguleux et ont un aspect fracturé. Nécrose tubulaire aigüe, inflammation tubulo-interstitielle et réaction focale à cellules géantes. |
Restriction des chaînes légères monoclonales (kappa ou lambda), quantités variables de dépôts d'uromoduline par IHC, démasquage par digestion à la pronase parfois nécessaire pour démontrer la composition monotypique des cylindres tubulaires. |
Matériel granulaire dense aux électrons pour la plupart non spécifique, avec des sous-structures cristallines occasionnelles. |
|
Amylose AL |
Amylose AL 21 % chez les patients atteints de myélome multiple [14]. Protéinurie importante (protéinurie médiane, 5 à 6 g/jour), syndrome néphrotique (66 %), maladie rénale chronique légère (créatinine médiane, 1,2 mg/dl). |
Dépôts hypocellulaires, amorphes, mésangiaux et capillaires pariétaux (type spiculaire), coloration pâle au PAS, PASM, rouge Congo positif avec biréfringence vert pâle (polarisé), TBM variable, rarement sous forme de cylindres, dépôts pariétaux interstitiels et artériels. |
Coloration pseudolinéaire à tachée pour la chaîne légère ou la chaîne lourde monotypique lambda > kappa (7 : 1) dans les dépôts amyloïdes. |
Fibrilles rigides, non ramifiées, orientées de façon aléatoire, de section transversale solide, remplaçant la matrice extracellulaire, d'un diamètre compris entre 8 et 12 nm |
|
TPCL |
4 à 5 % des autres maladies rénales liées à la dysprotéinémie. Protéinurie (protéine médiane, 1,5 à 2,5 g/jour), maladie rénale chronique légère (créatinine médiane, 1,9 à 2,0 mg/dl), tubulopathie proximale avec ou sans syndrome de Fanconi complet. |
Différents degrés de lésion des cellules tubulaires, perte des bordures en brosse, ballonnement ou pâleur cytoplasmique donnant un aspect spumeux par des dépôts granulaires H&E, PAS-négatifs et fuscinophiles, cytoplasmiques ou lysosomal (type non cristallin). Dépôts cristallins fuschinophiles PAS-positifs de formes variées (type cristallin). |
Coloration monoclonale aux chaînes légères kappa (type cristallin). Peut nécessiter un démasquage par digestion à la pronase sur des coupes de tissus incluses en paraffine pour confirmer le diagnostic. |
Dépôts tubulaires cytoplasmiques ou intralysosomalux amorphes, cristallins (en forme de bâtonnet, de losange ou d'aiguille) ou tubulo-fibrillaires observés, près d'un tiers des inclusions lysosomales non cristallines sont à chaîne légère lambda. |
|
Maladie de surcharge histiocytaire à cristaux |
Rare, avec environ 20 cas rénaux décrits dans la littérature [15]. Peut parfois survenir en combinaison avec d’autres conditions provoquant la MGRS [16]. Protéinurie (plage de protéines urinaires sur 24 heures : 2,4 à 4,6 g), fonction rénale réduite (plage de créatinine sérique : 2,38 à 5,01 mg/dL). |
Histiocytes interstitiels et glomérulaires contenant des inclusions cristallines hyperéosinophiles, cellules “pseudo-Gaucher”. |
Coloration positive pour les fragments d'Ig (le plus souvent IgG kappa LC), la coloration CD68 en IHC positive confirme le phénotype histiocytaire des cellules contenant les inclusions cristallines. |
Cristaux en forme d'aiguilles denses aux électrons dans les histiocytes de l'interstitium et des capillaires glomérulaires. |
|
Néphrite interstitielle tubulaire aiguë médiée par les chaînes légères (tubulopathie associée à une réaction inflammatoire interstitielle)[7] |
22 % des biopsies rénales liées à la dysprotéinémie monoclonale (28/126) dans une étude. AKI ou CKD, protéinurie non néphrotique. |
Inflammation interstitielle composée de lymphocytes et de plasmocytes disperses, avec des éosinophiles occasionnels. Lésions épithéliales tubulaires avec tubulite occasionnelle. |
Coloration granulaire aux chaînes légères monoclonales dans le cytoplasme des cellules tubulaires proximales accompagnée d'une coloration linéaire le long des membranes basales tubulaires dans les zones d'inflammation. 16/28 cas avec dépôts kappa et 12/28 cas avec dépôts restreints à chaîne légère lambda. |
Tubules avec des lysosomes cytoplasmiques proéminents et des signes de lésions tubulaires, généralement associés à des zones d'inflammation et de tubulite. Dans 7 cas, il y avait un dépôt focal de matériel ponctué dense aux électrons le long des membranes basales tubulaires |
Tableau 1. Résumé des MGRS courantes ainsi que de certaines lésions rénales non liées à la MGRS affectant principalement le compartiment tubulo-interstitiel (adapté avec les modifications de [6] et [9])
RÉFÉRENCES
- Leung N, Bridoux F, Batuman V, et al. The evaluation of monoclonal gammopathy of renal significance: a consensus report of the International Kidney and Monoclonal Gammopathy Research Group [published correction appears in Nat Rev Nephrol. 2019 Feb;15(2):121]. Nat Rev Nephrol. 2019;15(1):45-59. doi:10.1038/s41581-018-0077-4
- Stratta P, Gravellone L, Cena T, Rossi D, Gaidano G, Fenoglio R, et al. Renal outcome and monoclonal immunoglobulin deposition disease in 289 old patients with blood cell dyscrasias: a single center experience. Crit Rev Oncol Hematol. (2011) 79:31–42. 10.1016/j.critrevonc.2010.05.001
- Sayed RH, Wechalekar AD, Gilbertson JA, Bass P, Mahmood S, Sachchithanantham S, et al. Natural history and outcome of light chain deposition disease. Blood. (2015) 126:2805–10. 10.1182/blood-2015-07-658872
- Stokes MB, Valeri AM, Herlitz L, Khan AM, Siegel DS, Markowitz GS, D'Agati VD. Light Chain Proximal Tubulopathy: Clinical and Pathologic Characteristics in the Modern Treatment Era. J Am Soc Nephrol. 2016 May;27(5):1555-65. doi: 10.1681/ASN.2015020185. Epub 2015 Sep 15. PMID: 26374607; PMCID: PMC4849818.
- Larsen CP, Bell JM, Harris AA, Messias NC, Wang YH, Walker PD. The morphologic spectrum and clinical significance of light chain proximal tubulopathy with and without crystal formation. Mod Pathol. 2011;24(11):1462-1469. doi:10.1038/modpathol.2011.104
- Leung N, Bridoux F, Nasr SH. Monoclonal Gammopathy of Renal Significance. N Engl J Med. 2021;384(20):1931-1941. doi:10.1056/NEJMra1810907
- Herrera GA. Proximal tubulopathies associated with monoclonal light chains: the spectrum of clinicopathologic manifestations and molecular pathogenesis. Arch Pathol Lab Med. 2014;138(10):1365-1380. doi:10.5858/arpa.2013-0493-OA
- Luciani A, Sirac C, Terryn S, et al. Impaired lysosomal function underlies monoclonal light chain-associated renal Fanconi syndrome. J Am Soc Nephrol 2016;27:2049-2061
- Sy-Go JPT, Herrmann SM, Seshan SV. Monoclonal Gammopathy-Related Kidney Diseases. Adv Chronic Kidney Dis. 2022;29(2):86-102.e1. doi:10.1053/j.ackd.2022.01.004
- Kousios A, Blakey S, Moran L, et al. Non-crystalline light chain proximal tubulopathy, a morphologically protean entity [published online ahead of print, 2023 Apr 29]. Nephrol Dial Transplant. 2023;gfad085. doi:10.1093/ndt/gfad085
- Nasr SH, Fidler ME, Said SM. Paraffin Immunofluorescence: A Valuable Ancillary Technique in Renal Pathology. Kidney Int Rep. 2018 Jul 7;3(6):1260-1266. doi: 10.1016/j.ekir.2018.07.008. PMID: 30450452; PMCID: PMC6224795
- Büttner-Herold M, Krieglstein N, Chuva T, Minuth K, Pfister F, Daniel C, Klewer M, Büttner A, Ferrazzi F, Bertz S, Amann K. Light Chain Restriction in Proximal Tubules-Implications for Light Chain Proximal Tubulopathy. Front Med (Lausanne). 2022 Mar 28;9:723758. doi: 10.3389/fmed.2022.723758. PMID: 35419374; PMCID: PMC8995435.
- Hutchison CA, Heyne N, Airia P, Schindler R, Zickler D, Cook M, et al. Immunoglobulin free light chain levels and recovery from myeloma kidney on treatment with chemotherapy and high cut-off haemodialysis. Nephrol Dial Transplant. (2012) 27:3823–8. 10.1093/ndt/gfr773
- Nasr SH, Valeri AM, Sethi S, et al. Clinicopathologic correlations in multiple myeloma: a case series of 190 patients with kidney biopsies. Am J Kidney Dis. 2012;59(6):786-794. doi:10.1053/j.ajkd.2011.12.028
- Gupta RK, Rosenberg AZ, Bagnasco SM, Arend LJ. Renal crystal-storing histiocytosis involving glomeruli - A comprehensive clinicopathologic analysis. Ann Diagn Pathol. 2019;43:151403. doi:10.1016/j.anndiagpath.2019.151403
- Zhu L, Wang L, Shi H, et al. Combined crystal-storing histiocytosis, light chain proximal tubulopathy, and light chain crystalline podocytopathy in a patient with multiple myeloma: a case report and literature review. Ren Fail. 2023;45(1):2145970. doi:10.1080/0886022X.2022.2145970


